Historikk
Den første laparoskopiske nefrektomien ble utført allerede i 1990 av Clayman [1]. Operasjonstid opp mot 9 timer og mange komplikasjoner medførte at det tok lang tid før metoden ble akseptert. I dag regnes laparoskopisk nefrektomi som gullstandard av mange. Partiell nefrektomi (PN) ble først utført hos pasienter med absolutt indikasjon for nefronsparende kirurgi, hvor radikal nefrektomi ville medføre fullstendig tap av nyrefunksjonen. Dette gjelder pasienter med solitær nyre eller bilaterale tumores. Relative indikasjoner for nefronsparende kirurgi er tilstedeværelse av sykdom, eller risiko for sykdom, som forventes å gi redusert nyrefunksjon. I dag er den vanligste indikasjonen for PN tilstedeværelse av tumores med diameter opp til 4 cm og en normal kontralateral nyre. Flere studier viser likeverdig cancer kontroll ved PN og RN for tumores av slik størrelse [2,3]. To studier viser også at PN reduserer risiko for progresjon til nyresvikt sammenliknet med RN hos pasienter med normal kontralateral nyre [4,5].

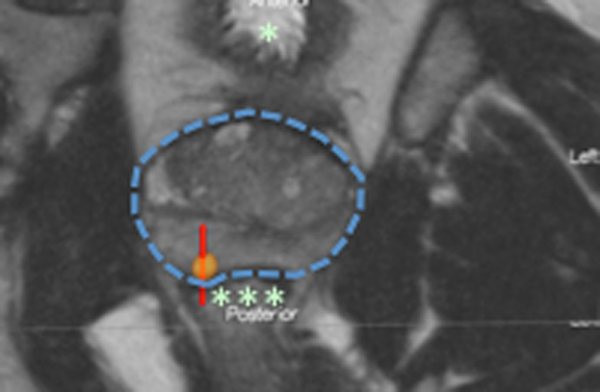
Bilde 1. CT av tumor
Diagnostikk
De fleste nyretumores oppdages i dag tilfeldig, da det er lav terskel for å rekvirere ultralyd undersøkelse eller CT av abdomen. Dette samsvarer godt med våre erfaringer, hvor 50 % av pasientene var uten symptomer ved diagnosetidspunkt. Tidlig diagnostikk gjør at de fleste nyresvulster er av liten størrelse ved påvisning. CT av nyren vil vanskelig kunne diskriminere mellom benign eller malign tumor. Det anbefales fremdeles ikke å utføre preoperativ biopsi av nyretumores, da det kan være usikkert om selve svulsten eller normalt nyrevev blir biopsert. Patologen vil også ha tolkningsproblemer ved små biopsivolum. Faren for implantasjonsmetastaser i stikk-kanalen er neglisjerbar. Nyere studier antyder imidlertid at biopsering av nyretumores har en akseptabel sensitivitet og spesifisitet. Således må man velge mellom å kontrollere pasienten med hyppige ultralyd eller CT undersøkelser for å se etter vekstøkning, eller å operere pasienten med nefronsparende teknikk. Det finnes også nomogrammer som kan brukes til å forutsi sannsynligheten for malignitet i tumor [6]. Yngre pasienter blir oftest operert, og eldre blir ofte anbefalt et konservativt kontrollregime.

Bilde 2. Karkontroll
Den første laparoskopiske partielle nefrektomi (LPN) ble utført av Winfield i 1992 [7] hos en pasient med godartet sykdom. Økning i kirurgiske ferdigheter har medført at LPN er blitt en etablert metode også for ondartete tumores på opptil 4 cm. Kritikere av metoden har hevdet at den er forbundet med en uakseptabel grad av komplikasjoner og ufrie kirurgiske marginer. Studier hvor man sammenligner LPN og PN viser imidlertid nærmest identiske resultater hva gjelder komplikasjoner og grad av ufrie marginer [8]. Denne og andre studier viser videre klare fordeler for LPN i forhold til PN når det gjelder blødning, bruk av postoperativ smertestillende, liggetid og tid til pasienten kan utføre vanlige aktiviteter [9].
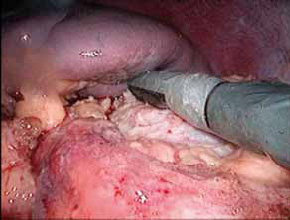
Bilde 3. Ultralyd probe
Operasjonsmetode
Vi har ved OUU de siste to og et halvt år behandlet 16 pasienter med små nyretumores med LPN, og jeg vil videre diskutere operasjonsmetoden. Pasientene undersøkes med preoperativ CT thorax for å utelukke metastatisk sykdom og CT abdomen med rekonstruksjon av nyrekar (bilde1). Operasjonen kan gjøres med transabdominal eller retroperitoneal tilgang. De fleste forfattere anbefaler en transabdominal teknikk, som gir bedre plass for suturering [10]. Den retroperitoneale teknikken kan brukes på mindre, dorsalt beliggende tumores [10]. Transabdominalt opereres pasienten i sideleie med lett nyreknekk. Det benyttes fire troacarer. Etter mobilisering av colon dissekeres karstilken til nyre. Det er ulike oppfatninger om man skal ”clampe” både arterien og venen eller bare arterien. I en spørreundersøkelse svarte 41 % at de clampet bare arterien, 31 % arterie og vene selektivt og 28 % arterie og vene samlet. Dr. Gill fra Cleveland Clinc, som er verdensledende på urologisk laparoskopisk kirurgi, anbefaler å clampe arterie og vene samlet med en Satinsky tang. Dermed reduseres risikoen for karskade og karspasme. [8]. Vår prosedyre har vært å clampe arterie og vene selektivt med Bulldog (bilde 2). Før clamping gis 250 ml Mannitol intravenøst.

Bilde 4. Ultralydbilde
Nyretumor identifiseres
Det er vanskelig å unngå å fjerne noe av det perirenale fettet for å få visualisert tumor. For å identifisere tumor og visualisere grensen mellom tumor og normalt nyrevev, anbefales bruk av peroperativ ultralyd. Det finnes på markedet ultralydsonder til bruk gjennom en 12 mm port. En studie viser reduksjon i ufrie marginer fra 14 % til 3 % ved bruk av peroperativ ultralyd. Vår erfaring med en pasient viser at sonden er enkel å bruke og gir oss mulighet til å påvise tumores som ikke er synlige på nyreoverflaten (bilde 3 og 4). Reseksjonskanten i nyrekapselen merkes med diatermi og tumor eksideres med kald saks. Nyere eksisjonsteknikker som laser og vannjet disseksjon, er fortsatt å regne som eksperimentelle. Disseksjon med diatermi skaper en forkullet reseksjonsflate som vanskeliggjør diskriminering mellom normalt og patologisk vev. Preparatet plasseres i en Endobag (plastpose til å legge preparatet i) for å unngå utsæd av cancerceller ved fjerning av preparatet (bilde 5). Samlesystemet sys med fortløpende Vicryl 2-0 (bilde 6). Deretter anbefales å applisere FloSeal (fibrinaktivator) og Surgicel. Vi har også brukt Surgicel og Tachosil. Nyrevevet adapteres avslutningsvis med en ny suturrekke før clampingen oppheves. Varm ischemitid i vårt materiale var i gjennomsnitt 27 minutter (11-39 min.). Dette er sammenlignbart med internasjonale resultater. [7]. Man bør bestrebe seg på oppnå ischemitid under 30 minutter. Eksperimentelle- samt kliniske studier imidlertid ingen redusert nyrefunksjon etter clamping opp mot 60 minutter [7]. Ved PN er det vanlig praksis å kjøle ned nyren ved å legge ”is-sludge” rundt nyren. En tilsvarende teknikk er ikke mulig ved LPN. Det har vært forsøkt med nedkjøling via et ureterkateter lagt opp i nyrebekkenet, men metoden er ikke etablert. Janetschek og medarbeidere har vist at det også er mulig å kjøle nyren med et laparoskopisk anlagt kateter i nyrearterien. Det har vært hevdet at ved åpning av samlesystemet bør det anlegges en JJ-stent for å redusere muligheten for postoperativ urinlekkasje. En studie av 103 pasienter viste imidlertid ingen effekt av innleggelse av JJ-stent [7]. Ingen av våre pasienter utviklet urinlekkasje, noe som er rapportert hos opptil 8 % av pasientene i andre studier [11]. Tumorer med diameter under 2 cm som ligger helt perifert, nærmest som en ”sopp”, kan fjernes uten sentral karkontroll. Slik tumor kan fjernes med diatermikniv eller ultracision [7]. Vi har forsøkt dette med godt resultat.

Bilde 5. Fjerning av tumor
Resultater
Det er ulike oppfatninger om bruken av peroperativ frysesnittdiagnostikk, og erfaringene er delte. Det vil samtidig være vanskelig å vurdere reseksjonskanten. Vi har ikke brukt peroperativ frysesnittdiagnostikk rutinemessig. Hos en pasient ble diagnosen endret fra godartet tumor peroperativt til malign tumor postoperativt med usikker fri margin. Det ble derfor gjort laparoskopisk nefrektomi, men det ble ikke påvist resttumor i preparatet. Vi har så langt ikke observert alvorlige komplikasjoner. Ingen pasienter er konvertert til PN eller laparoskopisk nefrektomi og ingen har fått blodtransfusjon. Gjennomsnittlig blodtap har vært 325 ml. En pasient fikk feber av ukjent årsak. Histologisk diagnose viste cancer hos 56 % av pasientene, noe som samsvarer med andres erfaring (60-70%) [11]. 44 % av pasientene har således i vårt materiale unngått å miste en hel nyre for godartet sykdom. Så langt har vi ikke sett tegn til lokalt eller metastatisk residiv.
Oppsummering
LPN kan benyttes hos pasienter hvor tumors diameter er opp mot 4 cm. Det anbefales transperitoneal teknikk, karkontroll med clamping, reseksjon med kald saks, lukking av nyren i to lag og bruk av hemostatisk substans. Metoden krever stor erfaring i laparoskopisk operasjonsteknikk.

Bilde 6. Suturering
Referanser
1 Clayman et al. Laparoscopic nefrectomy: initial case report. J Urol 1991; 146:278-82.
2 Hafez et al. Management of small solitary unilateral renal cell carcinomas. Impact of central versus peripheral tumor location. J Urol;1998:1156-60
3 Lerner et al. Disease outcome in patients with low stage renal cell carcinoma treated with nephron sparing or radical surgery. J Urol 2002;167: 884-90
4 McKiernan et al. Natural history of chronic renal insufficiency after partial and radical nefrectomy. Urology 2002. 59; 816-20
5 Lau et al. Matched comparison of radical nephrectomy vs. nephron-sparing surgery in patients with unilateral renal cell carcinoma and normal contralateral kidney. Mayo Clin Proc 2000;75:1236-42
6 Lene et al. J Urol 2007;178:429-36
7 Winfield et al. Laparoscopic partial nephrectomy. Initial case report for benign disease. J Endourol 1993;7: 521-6
8 Gill et al. Comparative analysis of laparoscopic versus open partial nephrectomy for renal tumors in 200 patients. J Urol 2003;170:64-8
9 Dunn et al. laparoscopic vs. open radical nephrectomy; a 9-years experience. J Urol 2000;164:1153
10 Wiese et al. Laparoscopic partial nefrectomy. J Urol 2007; 19:634-42.
11 Rassweiler et al. Laparoscopic partial nephrectomy: The European experience. Urol Clin North Am 2000;27:721- 26