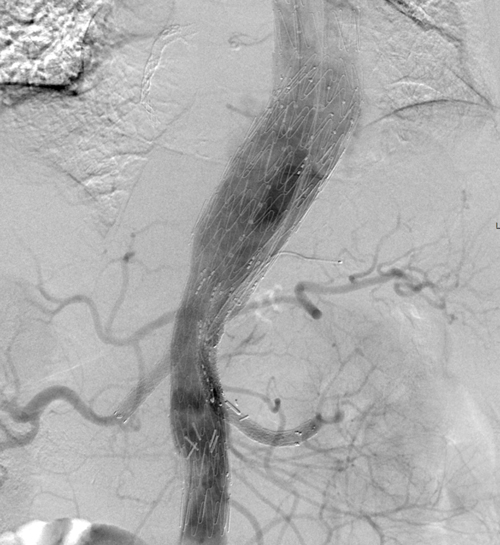
Ett stentgraft består av en kärlprotes av syntetisk väv (polyester eller polytetrafluoroethylene (PTFE)) som stöttas upp av en metallstent av rostfritt stål eller nitinol som vanligtvis är självexpanderande. Stentgraftet hålls på plats via stentets radiella kraft och kräver normalt landningszoner med förhållandevis frisk aorta både proximalt och distalt om aneurysmet. Några stentgraft har också tunna krokar ”barbs” eller ”hooks”. För fast förankring bör stentgraftets diameter överstiga aortas diameter vid landningszonerna med minst 10-15%.
Endovaskulär stentgraftbehandling av abdominala aortaaneurysm i Norge blev för första gången genomfört i Trondheim i 1995 (1). Endovaskulära tekniker har därefter fått en framträdande roll i hanteringen av aneurysm isolerade till infrarenala bukaorta (EVAR) och så småningom också i aorta descendens (TEVAR). Detsamma skulle också vara sant för det mellanliggande thorakoabdominella segmentet om det inte vore för komplexiteten i exkluderande av aneurysm från cirkulationen under bibehållande av flöde till dess grenar. På senare år har utvecklandet av modulbaserade stentgraft med sidohål (FEVAR) eller grenar (BEVAR) gjort det möjligt att också behandla thorakoabdominella aortaaneurysm. Den först behandlade patienten i Norge fick i Januari 2013 vid St Olavs sjukhus i Trondheim ett specialtillverkat grenat stentgraft. Det blev gjort reparation av et Crawford typ III aneurysm med sidogrenar till bukkärl och njurartärer. Idag blir denna typ av ingrepp utförda i samtliga helseregioner i Norge och fram till dags dato är det rapporterat mer än 30 st liknande procedurer i Norge.
Aneurysm –beskrivning och risk
Ett aneurysm är per definition en utvidgning av ett blodkärl ≥ 1.5 gånger normal storlek (diameter). När ett aneurysm ökar i storlek tenderar väggen att bli tunn med risk för ruptur.
Aorta descendensaneurysm (DTAA) involverar nedåtstigande aorta i bröstkorgen (men kan också helt eller delvis involvera aortabågen) och thorakoabdominella aortaaneurysm (TAAA) involverar i tillägg olika delar av abdominalaorta inklusive viscerala avgångskärl.
Risken förknippad med operativa ingrepp ökar med aneurysmets utbredning och det är därför viktigt att klassificera aneurysm därefter när man jämför olika behandlingsmetoder. (Figur 1).

Figur 1: Crawfords indelning av torakoabdominella aortaaneurysm, modifierat av Safi. Typ I startar direkt efter vänster a. subclavia och inkluderar hela aorta descendens och övre delen av abdominalaorta, vanligtvis till njurartärerna. Typ II går ut från samma nivå som typ I, men involverar hela thorakoabdominella aorta. Type III involverar distala delen av aorta descendens och hela abdominalaorta. Type IV involverar hela abdominalaorta från diafragma till aortabifurkaturen. Typ V involverar aorta från 6. interkostalrum till njurartärer.
Studier på naturalförlopp av thorakala aneurysm har visat att DTAA, i genomsnitt, tillväxer 0,19 cm per år. Når aortan har nådd 6 cm i diameter har patienten en årlig risk på ca 14% för dissektion, ruptur eller död. DTAA har en kritisk dimension på ca 7 cm där risken för framtida dissektion eller ruptur ökar till ca 43%. KOLS, hög ålder och smärta är visat vare medverkande riskfaktorer. I en väldefinierad patientpopulation med TAAA, följd över 30 år, drabbades 73% av patienterna av ruptur. I ett annat klassiskt patientmaterial med TAAA och kontraindikationer för kirurgi, levde endast 25% av patienterna efter 2 års uppföljning. I ytterligare studier med konservativt följda TAAA (> 6 cm) är 5-års överlevnad 39% och reparationsfri överlevnad 17%. (2-6)
Till samman ger ackumulerade data starkt stöd en för en aggressiv hållning med förebyggande kirurgiska behandling av asymtomatiska aneurysm i aorta descendens och thorakoabdominella aorta för att förhindra dissektion, ruptur och för tidig död.
I de senaste europeiska guidelines för aortasjukdom (7) rekommenderas: TEVAR bör värderes hos patienter med DTAA med maximal diameter >55 mm (evidensnivå IIa,C). När TEVAR icke är teknisk möjlig bör kirurgi värderas hos patienter som har DTAA med maximal diameter >60 mm (IIa,C). När intervention är indicerad vid Marfans syndrom eller andra vävnadsdefekter bör öppen kirurgi värderas i stället for TEVAR (IIa,C). Symptomatiska aneurysm måste opereras oavsett storlek. Familjemedlemmar bör undersökas för eventuella asymtomatiska aneurysm.
 Stentgraft för DTAA och TAAA
Stentgraft för DTAA och TAAA
De potentiella fördelarna med en minimal invasiv endovaskulär metod är uppenbara. Pasienten undgår thorakolaparotomi och avstängning av aorta och metoden ger minimal organischemi. I teorin innebär den endovaskulära proceduren mindre stress på patienten, vilket bör leda till mindre dödlighet och sjuklighet.
Utvecklingen av Endovaskulära metoder går raskt framåt och grafter och metoder blir bättre och bättre. Idag är i stort sett hela aorta tillgänglig för endovaskulär intervention och det är få kontraindikationer. För bäst resultat behandlas aneurysm med normal aorta/kärl i varje fästezon. Europeiska guidelines (7) rekommenderar fästezon med aortadiameter ≤40 mm och längd ≥2 cm för TEVAR. Vid EVAR bör den proximala aortahalsen ha en längd av minst 10 till 15 mm och ≤32 mm i diameter. Dock har det successivt kommet tillpassningar som gör att många flera typer av aneurysm kan behandlas och antalet olika ”devicer” ökar med jämn takt.
De flesta DTAA kan idag med fördel behandlas med tubulära stentgraft (Figur 2). Problem kan vara att aorta descendens gör en skarp böj eller har avsaknad av hals opp mot halskärlen. Det er då vanligt at man täcker vä subclavia artärens avgång för att få gott fäste upptill (ofta karotis-subklavia bypass innan). Med hjälp av extraanatomiska bypass till den cerebrala cirkulationen ”arch debranching” kan man idag också behandla aneurysm som börjar högt upp i aortabågen.
TAAA involverar som oftast bukkärl och njurartärer. Utvecklingen av endovaskulär behandling har lett fram till modulära grenade och fenestrerade stentgraftsystem.
Modulära stentgrafter monteras inne i pasienten från flera komponenter. Alla nuvarande flergrenade modulära stentgraft kombinerar storkalibriga självexpanderande stentgrafter med finkalibriga täckta bro-stentgrenar. De skiljer sig i typen av interkomponent anslutning. BEVAR innebär en överlappande förbindelse mellan en självexpanderande täckt bro-stent och kaudalt riktade manschetter anslutna till det primära stentgraftet (Figur 3). Tekniken är idealisk för grenar ifrån stora aortalumen såsom trunkus celiakus och arteria mesenterica superior. BEVAR passar ofta bra för alla 4 viscerala kärl vid TAAA där aneurysmet omfattar njurartärernas avgångar (Crawford typ II-IV).
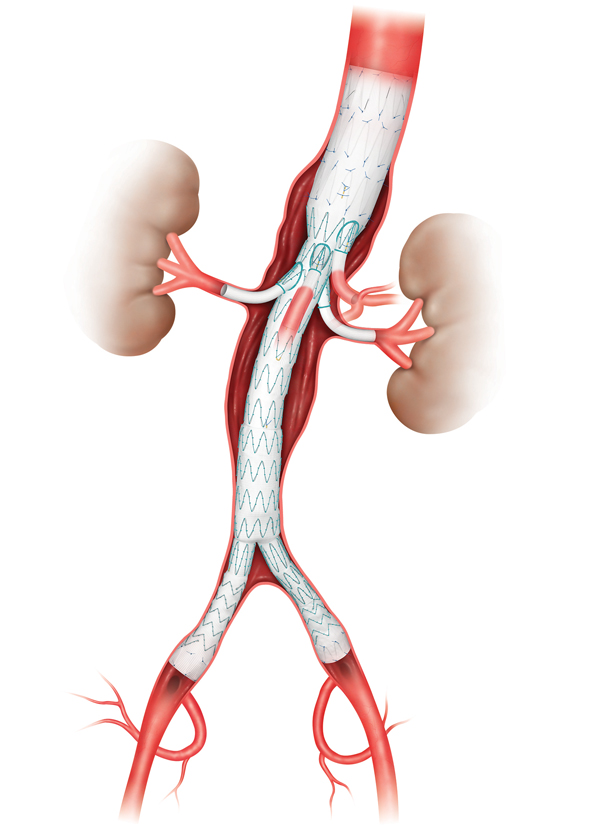
En nackdel med BEVAR och FEVAR är att graften är mycket kostbara och måste specialutformas efter varje patient med en beställningstid på flera veckor. Det sista året har det dock kommit ett ”off-the–shelf” standardiserat grenat stentgraft (eg Zenith® T-Branch, Cook Medical)(Figur 5) som är bedömt kunna fungera på 70-80% av patientpopulationen.
Öppen kirurgi
Det er många utmaningar knutna till öppen kirurgisk behandling av TAAA. Reparation av thorakoabdominella aorta medför ett stort kirurgiskt trauma då man för tillgång måste öppna både bröstkorg och buk (thorakolaparatomi). Operationen medför ofta stor perioperativ blödning och risk för ischemiska komplikationer för involverade organsystem. Till exempel är cirkulationen till ryggmärgen helt beroende av vissa interkostalartärer respektive lumbalartärer med stor interindividuell variation och risk för ryggmärgsischemi när aneurysmet exkluderas. En fruktad komplikation till TAAA operation är därför paraparese eller paraplegi. Andra viktiga komplikationer är affektion av njur- hjärt- och lungfunktion och multiorgansvikt

Under de siste 25 åren har det skett flera tekniska framsteg, bland annat med bruk av hjärt-lungmaskin för distal perfusion av aorta och olika metoder för protektion av ryggmärg och inre organ. Den initiala frekvensen av ryggmärgsskada i upp mot 40% för dom mest utbredde aneurismen har med hjälp av distal aortaperfusion och dränage av spinalvätska kunnat minskas till mindre än 10% vid center med hög volym (9).
Kirurgisk tillgång vid TAAA har dock fortsatt behov av bred aorta exponering via thorakolaparatomi och ett visst avbrott i flödet till bukorganen som har liten tolerans för ischemi. Ingreppen är fortsatt stora och komplicerade operationer som fortsatt utgör en stor påfrestning för patienterna och kan vara förenade med stor risk för komplikationer. Ofta är patienter med TAAA äldre och hjärt- och lungsjuka i tillägg och många kan därför inte erbjudas operation. Samhällsekonomiskt medför postoperativ vård och rehabilitering betydande kostnader. Sammantaget är detta goda skäl att finna ett mindre invasivt, endovaskulärt alternativ till öppen kirurgisk reparation av TAAA .
Procedur för behandling av TAAA med grenat stentgraft (St Olavs hospital)
Patienten är i full narkos och har ett preoperativt inlagt spinaldränage. Proceduren utförs i tätt samarbete mellan interventionsradiolog, kärlkirurg, thoraxkirurg och anestesiläkare. Tillgången till artärsystemet sker rutinmässigt via kirurgisk åtkomst av femoralis artären i bägge ljumskar. Dessutom görs en tredje incision för att få tillgång till axillaris artären som senare kommer att användas till att införa de viscerala stentgraften. Huvudkomponenterna läggs opp från femoralartären. Kärlet som används måste kunna härbärgera den vaskulära införingshylsan som stentgraftet ligger i vid leverans (22 Fr./8,5 mm). Eventuellt läggs först ett thorakalt stentgraft för att försegla den proximala delen av aneurysmet och skapa en optimal landningszon för det grenade stentgraftet. Det grenade graftet placeras noga i förhållande till aktuella målkärls avgångar så att varje visceral manschettgren landar ca 2 cm proximalt om öppningen av målartären (figur 7). Vid eventuell fenestrering läggs bro-stentgraften upp via tillgång från femoralis artären på kontralateral sida. Slutligen görs eventuell aorto-biiliakal förlängning och därefter stängs arteriotomierna i bägge femoralisartärer. Vid lång avstängning av cirkulationen till underextremiteter bör shuntning eller annat tilltag värderas. När huvudkomponenterna är på plats får man ett avsiktligt endoläckage genom stentgraftets grenar. Detta ger visceral perfusion via aneurysmsäcken medan bro-stentgraften implanteras via axillaris tillgången. Först kateteriseras manschetten i stentgraftet och därefter den aktuella viscerala grenen
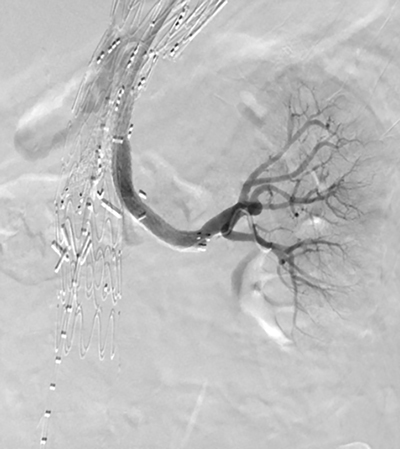
Efter att alla bro-stentgraft är på plats (Figur 10) görs en kontrollangiografi för att identifiera eventuellt endoläckage och bekräfta perfusion av varje visceralartär (Figur 11). Post-operativt väcks patienten på operationssal och övervakas på intensivvårdsavdelning första dygnet. Patienten har kvar spinaldränage i 3 dygn. Patienten följs postoperativt i vanligt protokoll för endovaskulära procedurer (Figur 12).
Resultat och tankar om framtiden
Erfarenheterna hitintills är att det är tekniskt möjligt at behandla TAAA med BEVAR och FEVAR. Man har tidigare varit helt beroende av specialtillverkade grafter men nu finns standardiserade graft som kan passa till många patienter. Kostnaden för behandlingen är hög och en operation kostar ofta mer än en halv miljon norska kronor. Metoden har en klar potential som alternativ till öppen operation. Patienterna tål även långa operationer väl och kan oftast bli väckta och extuberade direkt efter operationen. Det kirurgiska traumat är väsentligen mindre men problemet med paraplegi kvarstår i ungefär lika stor grad som vid öppen kirurgi beroende av att man täcker över interkostalärtärer och lumbalartärerer som försörjer ryggmärgen. Patienterna är ofta generellt kärl-, hjärt- och lungsjuka och behöver intensivvård första dygnen efter operationen och därefter noggrann 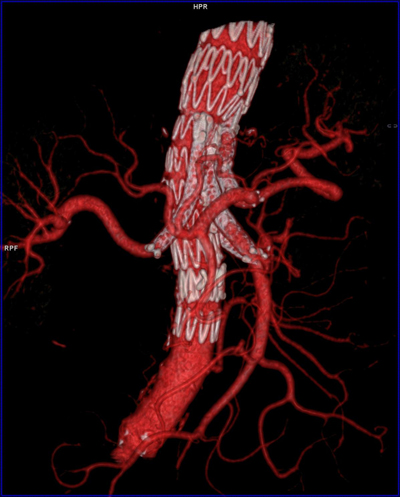
Sammantaget kommer endovaskulär behandling sannolikt spela en viktig roll vid behandling av TAAA, medan öppen kirurgi fortfarande är nödvändig hos vissa patienter. Kirurgisk behandling av aortasykdom har traditionellt delats upp i nivå med diafragma mellan thoraxkirurger och kärlkirurger och TAAA har behandlats i samarbete. Endovaskulär behandling har utvecklats i mångårigt samarbete mellan interventions radiologer och kärlkirurger. Patienter med TAAA förtjänar en noggrann utredning och att behandlingen skräddar sys efter vad patienten behöver och inte bara efter vilken metod som finns tillgänglig lokalt. Ett gränsöverskridande samarbete vid behandlingen av TAAA är helt i enlighet med de nya europeiska riktlinjerna (7) där man lyfter fram värdet av en helhetssyn på aorta som ett helt organ med behov av tvärvetenskaplig bedömning och man efterlyser behandling anpassad till den enskilde patienten på specialiserade centra.
Referanser
- Hatlinghus S, Dahle LG, Nordby A et al. Endovaskulær behandling av abdominale aortaaneurismer. TDnlf 1996;116:717-20
- Elefteriades JA. Natural history of thoracic aortic aneurysms: indications for surgery, and surgical versus nonsurgical risks. Ann Thorac Surg 2002;74:S1877-80
- Cambria RA, Gloviczki P, Stanson AW et al. Outcome and expansion rate of 57 thoracoabdominal aortic aneurysms managed non-operatively. Am J Surg 1995;170:213e7.
- Bickerstaff LK, Pairolero PC, Hollier LH et al. Thoracic aortic aneurysms: a population-based study. Surgery. 1982; 92(6):1103-8.
- Crawford ES, DeNatale RW. Thoracoabdominal aortic aneurysm: observations regarding the natural course of the disease. J Vasc Surg. 1986; 3(4):578-82.
- Natural History of Descending Thoracic and Thoracoabdominal Aneurysms. Griepp RB, Ergin A. Galla JD et al. Ann Thorac Surg 1999;67:1927–30)
- 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: Document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC). Erbel R, Aboyans V, Boileau C et al Eur Heart J. 2014; 35(41):2873-926.
- Crawford ES. Thoraco-abdominal and abdominal aortic aneurysms involving renal, superior mesenteric, and celiac arteries. Ann Surg 1974; 179: 763–72.
- Distal Aortic Perfusion and Cerebrospinal Fluid Drainage for Thoracoabdominal and Descending Thoracic Aortic Repair: Ten Years of Organ Protection. Hazim J. Safi, Charles C. Miller, III, Tam T.T. Huynh, et al. Ann Surg. 2003; 238(3): 372–381.
- O’Callaghan A, Mastracci TM, Eagleton MJ. Staged endovascular repair of thoracoabdominal aortic aneurysms limits incidence and severity of spinal cord ischemia. J Vasc Surg 2015; 61(2):347-354.
Tillåtelse för användning av bilder på stentgraften är beviljad av Cook Medical, Bloomington, Indiana.


 Stentgraft för DTAA och TAAA
Stentgraft för DTAA och TAAA